Page 548 - Advanced Organic Chemistry Part B - Reactions & Synthesis
P. 548
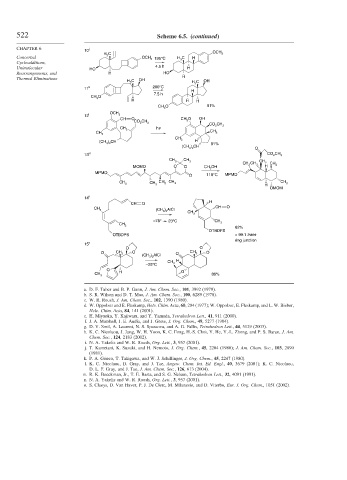
522 Scheme 6.5. (continued)
CHAPTER 6 j
10
H 3 C OCH 3
Concerted OCH 3 195°C H 3 C H
Cycloadditions,
Unimolecular HO 4.5 h H
Rearrangements, and H HO
Thermal Eliminations OH H
H 3 C H 3 C OH
11 k 200°C
H
7.5 h
CH 3 O
H H H
CH 3 O 91%
12 l OCH 3
CH O CH 3 O OH
CO 2 CH 3
CO 2 CH 3
hv
CH 3
CH 3
CH 3
CH 3
(CH 3 ) 2 CH H 91%
(CH 3 ) 2 CH
O
m
13 CO 2 CH 3
CH 3 CH 3
CH 2
CH 3 CH 3 CH 3
MOMO O O CH 3 OH H
MPMO
O 110°C MPMO
CH 3 CH 3 CH 3
CH 3
CH 3
H
OMOM
14 n
H
CH O
CH O
(CH 3 ) 2 AlCl
CH 3
CH 3
–78° 23°C CH 3
CH 3
62%
OTBDPS
OTBDPS > 99:1 trans
ring junction
o
15
O O
O CH 3 O O CH 3 O
(CH 3 ) 2 AlCl
H
CH 3
–25°C
O
H O
CH 3 86%
a. D. F. Taber and B. P. Gunn, J. Am. Chem. Soc., 101, 3992 (1979).
b. S. R. Wilson and D. T. Mao, J. Am. Chem. Soc., 100, 6289 (1978).
c. W. R. Roush, J. Am. Chem. Soc., 102, 1390 (1980).
d. W. Oppolzer and E. Flaskamp, Helv. Chim. Acta, 60, 204 (1977); W. Oppolzer, E. Flaskamp, and L. W. Bieber,
Helv. Chim. Acta, 84, 141 (2001).
e. H. Miyaoka, Y. Kajiwara, and Y. Yamada, Tetrahedron Lett., 41, 911 (2000).
f. J. A. Marshall, J. E. Audia, and J. Grote, J. Org. Chem., 49, 5277 (1984).
g. D. V. Smil, A. Laurent, N. S. Spassova, and A. G. Fallis, Tetrahedron Lett., 44, 5129 (2003).
h. K. C. Nicolaou, J. Jung, W. H. Yoon, K. C. Fong, H.-S. Choi, Y. He, Y.-L. Zhong, and P. S. Baran, J. Am.
Chem. Soc., 124, 2183 (2002).
i. N. A. Yakelis and W. R. Roush, Org. Lett., 3, 957 (2001).
j. T. Kametani, K. Suzuki, and H. Nemoto, J. Org. Chem., 45, 2204 (1980); J. Am. Chem. Soc., 103, 2890
(1981).
k. P. A. Grieco, T. Takigawa, and W. J. Schillinger, J. Org. Chem., 45, 2247 (1980).
l. K. C. Nicolaou, D. Gray, and J. Tae, Angew. Chem. Int. Ed. Engl., 40, 3679 (2001); K. C. Nicolaou,
D. L. F. Gray, and J. Tae, J. Am. Chem. Soc., 126, 613 (2004).
m. R. K. Boeckman, Jr., T. E. Barta, and S. G. Nelson, Tetrahedron Lett., 32, 4091 (1991).
n. N. A. Yakelis and W. R. Roush, Org. Lett., 3, 957 (2001).
o. S. Claeys, D. Van Haver, P. J. De Clerc, M. Milanesio, and D. Viterbo, Eur. J. Org. Chem., 1051 (2002).